

 |
 |
|
|
Навигация
Популярное
|
Публикации «Сигма-Тест» Теория горения 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 [ 42 ] 43 44 45 46 47 48 49 50 51 52 53 54 55 56 57 58 59 60 61 62 63 64 65 66 67 68 69 70 71 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86 87 88 89 90 91 92 93 94 95 96 97 98 99 100 101 102 103 104 Аналогично можно получить выражение для кинцеигра-цШ! азота: п= (4-24) Уравнения (4-23) н (4-24) справедливы в том случае, когда коэффициенты диффузии всех газов, коицен грации которых входят в уравнения, равны между собой. Хотя это предпо-.поженне никогда не выполняется полностыо, но для большинства газов оно вполне обосновано. Водород, однако, значительно легче других газов и имеет соответственно значительно больший коэффициент диффузии. Уравнение (4-23) поэтому дает, по-видимому, завышенное значение кон-иеитрации водорода на поверхности; в действительности m j должно быть меньше, так как больше, Б турбулентном потоке все газы, конечно, имеют одинаковое эффективное значение коэффициента диффузии, так что теория в этом случае должна быть очень близка к истине. Пример 4-2, Определить состав газа иа повсрхиостп углерода в примере 4-1. Решение. В состав газа входят СО, и N. Применяя следствие п- к соответственно к сохраняемым свойствам 12 , 12 2 -28 со+тг со;. ii,+Ts н.о; N. и полагая получн.м: 28 cos I 4- В так тто cos = 0.380, -.0,05+0 и,.- И-й - 0,005, 0,73 + 0 Таким образом, на поверхности газ имеет следующий весовой состав; 3*% СО, 0,5Уо Hj и 61,5% Na- Состав газа остается постоянным Моль трубы при условии, конечно, что выполняется предпосылка no = co,s = ii.os = 0- Состав газа вблизи и о в е р х и о с т и. Следует подчеркнуть, что при выводе выражения для В не было сделано никаких предноложений о том, как распределяется кислород между окисью углерода и углекислотой в любой точке, кроме иоверхиости топлива. В рассмотренном примере осталось ие выясненным, в каком виде выходит углерод из трубы: в виде окиси углерода или углекислоты. Расход углерода от этого ие зависит. Также осталось не-онределенным относительное количество кислорода, всту-11Ившего в соединение с углеродом и во,тородом. 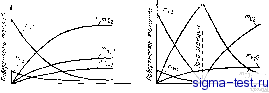 Расстяиие от noSesxnocmu i Расстояние о/т> noSepzmcmu топлива Рис. 4-8. Распределений концентраций в газе у поверхности углерода при высокотемпературном режи.\(е. а ~ ари отсутствии реакци(1 и:-гаэовой1)азс-: б-гфн наличии ргакци:: в газовой фазе На рис. 4-8,а и б представлены возможные распределения состава газа вблизи поверхности углерода. Рнс. 4-8Д соответствует отсутствию реакцн:! в газовой фазе: О2, COg] и НоО диффундируют к иоверхиости углерода, на которой, образ.уются СО и Но, диффунднручогдпе а свою очередь в об-( ратном направлении. Рис. 4-8,6 соответствует наличию вб.оизи ловерх]юсти топлива зоны реакции: с одной стороны к ней диффундирует О2, с другой - СО; образовавшая- ся в зоне реакции СО2 диффундирует как к иоверхност! углерода, где она реагирует в СО, так и обратно в газовый ноток: водород, образующийся па поверхности углерода, вновь окисляется в зоне реакции. Поскольку здес& рассматриваются только условия массообмена, то может с)ществоватъ .множество распределеитгй, подобных показанным на рис. 4-8, не оказывающих влияния на скорость переноса массы, за исключением косвенного - через изменение вязкости и т. п. Существование в ряде случаев 301% реакции подтверждается наличием голубого ореола вб круг горящего углерода и тем, что обычно СО не обнарУ* r.i2 живается в газовом потоке до тех пор, пока не будет израсходована большая часть кислорода. Протекание реакции в газовой фазе моя<ет быть предотвращено, например, добавлением в газ ингибитора, как это было осуществлено в носледовагшях Артура, Бсигама н Бауринга (Arthur, Bangham and Bowring, 1949) и Мертенса я Гел.чицкса (Mertens and Hellinckx, 1949). Отрицание возможности существования составов газа, соответствующих как случаю а, так и случаю б на рис. 4-8, явилось иричиной многочисленных и сложных обсуждений вопроса о том, что является первичны.м продуктом горения- окись углерода или уг.теккслота. Действительно, для случая, когда углерод имеет умерещтую температуру и его реакциоиная способность по отношению к кислороду и углекислоте невысока и неодинакова, механизм горения еще не установлен. При высоких же температурах поверхности рассмотренный выше метод расчета скорости горения следует считать обоснованным. По всей вероятности, такой механизм процесса следует принять в качестве нор-ма.льного и изучать .отклоиенпя от него при реальном течении ироцесса в различных условиях. Пример 4-3. Опрсде.тигь соотаи газа, вы.кодя icero аз трубы в условиях примера 4-1. Решение. Единственного решения атой задаяп ие существует. Наиболее обосновано предположение (определяющее возможность решения), ято отходяни1е газы на.ходятся в термодинамическом рав-иовеснн. Здесь мы просто предположим, что отсутствует свободный водород и что одновременное содержание в газах кислорода и окиси углерода невозмон<но. Концентрацию пара на выходе найдем на основаЕ!ии п. з (стр. 1U6) и уравнения (4-17), которое дает 0,05 1,048 - 1,188 чьо = 0.044. Ь*сл[1 есть избыток кислорода, то в отходящих газах отсутствует СО-Тогда из баланса углерода [п. ж и уравнение (4-18)] получим; 12 ]2 ТГсо, ТГ- . 2 0,1880,0-18 ~ I 1ХЯ. I П.1Я Ь ],048 ~ ]J88 J,J88J,0-!S
|
|
© 2010 www.sigma-test.ru Санкт-Петербург: +7 (812) 265-34-48, +7 (812) 567-94-10
Разработка и поддержка сайта: +7(495)795-01-39 после гудка 148651, sigma-test.ru(my_love_dog)r01-service.ru Копирование текстовой и графической информации разрешено при наличии ссылки. |